Datos técnicos
| Fórmula | C28H30CIN5O4S |
||||||
| Peso molecular | 568.09 | Número CAS | 658084-23-2 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 92 mg/mL (161.94 mM) | ||||
| Ethanol | 2 mg/mL (3.52 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | SU11274 (PKI-SU11274) es un inhibidor selectivo de Met (c-Met) con una IC50 de 10 nM en ensayos libres de células, sin efectos sobre PGDFRβ, EGFR o Tie2. Este compuesto induce la autophagy, la apoptosis y la detención del ciclo celular. | ||
|---|---|---|---|
| Objetivos |
|
||
| In vitro | SU11274 exhibe una selectividad más de 50 veces mayor para Met en comparación con Flk y más de 500 veces mayor en comparación con otras Protein Tyrosine Kinase como FGFR-1, c-src, PDGFbR y EGFR. Este compuesto inhibe la fosforilación de reguladores clave de la vía PI3K, incluidos AKT, FKHR o GSK3β. El tratamiento con este químico inhibe el crecimiento de células BaF3 transformadas con TPR-MET de manera dependiente de la dosis con una IC50 de <3 μM en ausencia de interleucina 3, sin inhibición del crecimiento de células BaF3 transformadas por otras Protein Tyrosine Kinase oncogénicas, incluidas BCR-ABL, TEL-JAK2, TEL-ABL y TEL-PDGFβR. Además del crecimiento celular, el tratamiento con este compuesto inhibe significativamente la migración de las células BaF3. TPR-MET en un 44,8% y un 80% a 1 μM y 5 μM, respectivamente. Inhibe la fosforilación de Met dependiente de HGF, así como la proliferación y motilidad celular dependientes de HGF con una IC50 de 1-1,5 μM. En las células H69 y H345 que tienen un receptor Met funcional, este inhibidor inhibe el crecimiento celular inducido por HGF con una IC50 de 3,4 μM y 6,5 μM, respectivamente. Induce la detención del ciclo celular en G1 con un aumento de las células en fase G1 del 42,4% al 70,6% a 5 μM, e induce la apoptosis dependiente de caspasa en un 24% a 1 μM. Este compuesto inhibe la viabilidad celular en células de cáncer de pulmón no microcítico (NSCLC) que expresan c-Met con valores de IC50 de 0,8-4,4 μM, y anula la fosforilación de c-Met y su señalización descendente inducida por el factor de crecimiento de hepatocitos. |
Protocolo (de referencia)
| Ensayo de quinasa:[1] |
|
|---|---|
| Ensayo celular:[2] |
|
Referencias
|
Validación de productos por parte del cliente
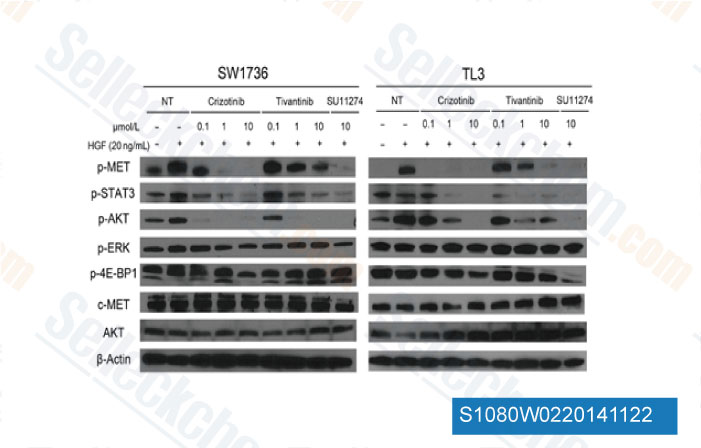
-
Datos de [ Mol Cancer Ther , 2014 , 13(1), 134-43 ]
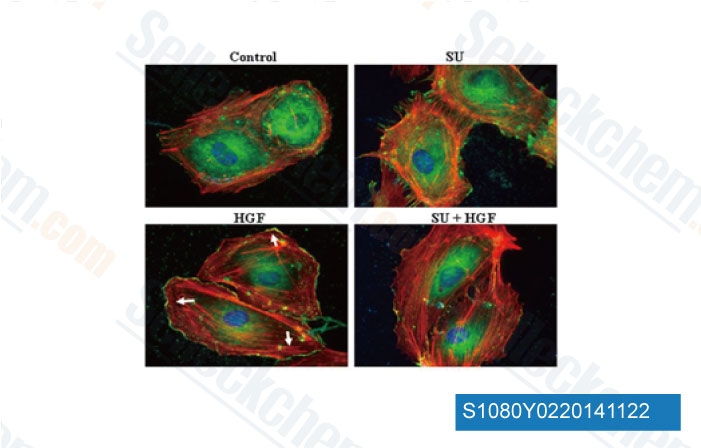
-
Datos de [ J Biol Chem , 2014 , 289(19), 13476-91 ]
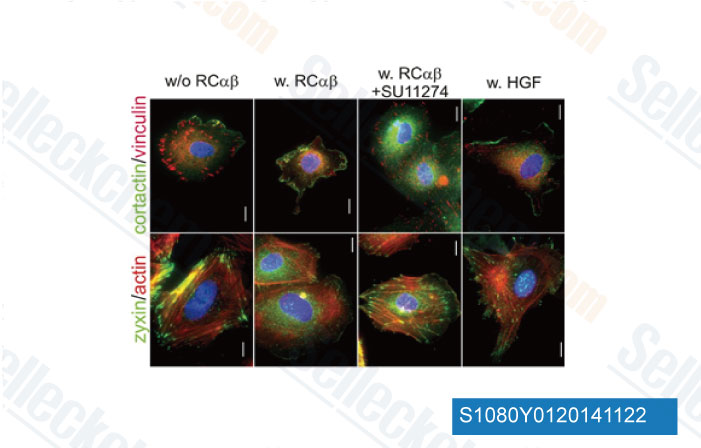
-
Datos de [ Arterioscler Thromb Vasc Biol , 2013 , 33(3), 544-54 ]
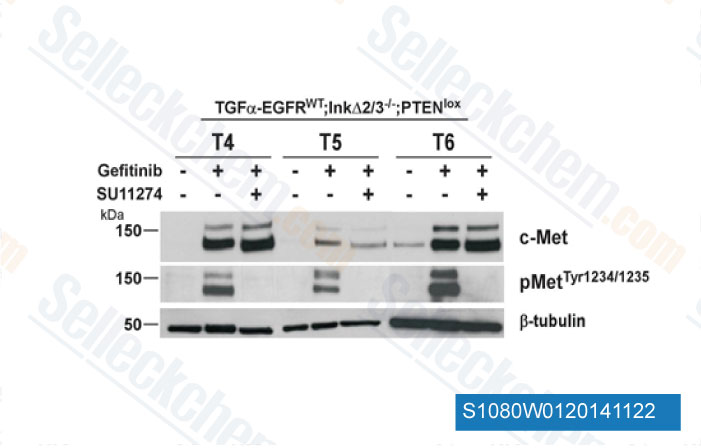
-
Datos de [ Oncogene , 2012 , 31(25), 3039-50 ]
Sellecks SU11274 Ha sido citado por 68 Publicaciones
| Inhibition of TFF3 synergizes with c-MET inhibitors to decrease the CSC-like phenotype and metastatic burden in ER+HER2+ mammary carcinoma [ Cell Death Dis, 2025, 16(1):76] | PubMed: 39920140 |
| Establishment and characterization of a new human gallbladder cancer cell line, OCUG-2 [ World J Exp Med, 2025, 15(2):100443] | PubMed: 40546672 |
| The anti-tumor effects of AZD4547 on ovarian cancer cells: differential responses based on c-Met and FGF19/FGFR4 expression [ Cancer Cell Int, 2024, 24(1):43] | PubMed: 38273381 |
| Establishing a new human lung squamous cell carcinoma cell line, OMUL-1, expressing insulin-like growth factor 1 receptor and programmed cell death ligand 1 [ Thorac Cancer, 2024, 10.1111/1759-7714.15488] | PubMed: 39552203 |
| Hepatocyte growth factor promotes retinal pigment epithelium cell activity through MET/AKT signaling pathway [ Int J Ophthalmol, 2024, 17(5):806-814] | PubMed: 38766346 |
| Epithelial cell adhesion molecule (EpCAM) regulates HGFR signaling to promote colon cancer progression and metastasis [ J Transl Med, 2023, 21(1):530] | PubMed: 37543570 |
| Met-signaling Controls Dendritic Cell Migration in Skin by Regulating Podosome Formation and Function [ J Invest Dermatol, 2023, S0022-202X(23)00100-8] | PubMed: 36813160 |
| Integrative analysis of drug response and clinical outcome in acute myeloid leukemia [ Cancer Cell, 2022, S1535-6108(22)00312-9] | PubMed: 35868306 |
| Resistance to tyrosine kinase inhibitors promotes renal cancer progression through MCPIP1 tumor-suppressor downregulation and c-Met activation [ Cell Death Dis, 2022, 13(9):814] | PubMed: 36138026 |
| β2-adrenergic receptor promotes liver regeneration partially through crosstalk with c-met [ Cell Death Dis, 2022, 13(6):571] | PubMed: 35760785 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
