Datos técnicos
| Fórmula | C27H29N5O |
||||||
| Peso molecular | 439.55 | Número CAS | 475489-16-8 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 88 mg/mL (200.2 mM) | ||||
| Ethanol | 24 mg/mL (54.6 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | NVP-AEW541 es un potente inhibidor de IGF-1R/InsR con una IC50 de 150 nM/140 nM en ensayos sin células, mayor potencia y selectividad para IGF-1R en un ensayo basado en células. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
|||||||||||
| In vitro | NVP-AEW541 también inhibe InsR, Tek, Flt1 y Flt3 con IC50 de 140 nM, 530 nM, 600 nM y 420 nM en ensayos de quinasas purificadas/dominios de quinasas recombinantes. Este compuesto es más selectivo y muestra una potencia 27 veces mayor que InsR a nivel celular. Suprime la supervivencia, el agar blando y la proliferación de células MCF-7 mediadas por IGF-I con IC50 de 0,162 μM, 0,105 μM y 1,64 μM, respectivamente. Este químico también reduce el nivel de fosfo-IGF-1R y fosfo-PKB en células NWT-21. Muestra un efecto inhibidor del crecimiento en células de sarcoma musculoesquelético TC-71 en medio con bajo suero, así como en medio que contiene 10% de FBS. Este compuesto inhibe la progresión del ciclo celular e induce una detención G1 específica en líneas celulares de sarcoma (TC-71, SK-N-MC, SaoS-2, RD/18 y RH4). Podría inhibir el crecimiento de células de neuroblastoma humano con IC50 de 0,4-6,8 μM. Se pudo detectar un aumento en la fracción hipodiploide y el agotamiento de los compartimentos S y G2-M en estas líneas celulares. Esta inhibición de IGF-1R impulsada por el compuesto causa una reducción de la fosforilación de Akt, pero no de Erk1 y Erk2 en células de neuroblastoma. Inhibe el crecimiento de células de glioma y altera el bucle autocrino iniciado por la estabilización de HIF1α. Un estudio reciente muestra que este químico suprime la proliferación y viabilidad de las células de cáncer de próstata PC3, DU145 y 22Rv1, sin necesidad de muerte celular asociada. Disminuye los niveles de fosfo-Akt en células 22Rv1 y DU415, pero no en células PC3, sin afectar los niveles totales de Akt, lo que demuestra que el estado de PTEN podría determinar la eficacia de este compuesto con Akt esencial. Esta radiosensibilización inducida por el compuesto depende del estado de activación de Akt. Podría aumentar la fosforilación de H2AX (una medida de DSBs) en células PC3, DU145 y 22Rv1. | |||||||||||
| In vivo | NVP-AEW541 (50 mg/kg, p.o.) da como resultado la abrogación del receptor basal e inducido por IGF-I, y la fosforilación de PKB y MAPK, con un valor T/C del 14% en el xenoinjerto tumoral NWT-21. Este compuesto (50 mg/kg) provoca la reducción del tumor en los xenoinjertos HTLA-230 y SK-N-BE2c, sin signos de toxicidad sistémica. Podría inhibir la invasión tumoral tanto en cámaras recubiertas de Matrigel como en xenoinjertos HTLA-230. |
Protocolo (de referencia)
| Ensayo de quinasa:[1] |
|
|---|---|
| Ensayo celular:[1] |
|
| Estudio en animales:[1] |
|
Referencias
|
Validación de productos por parte del cliente
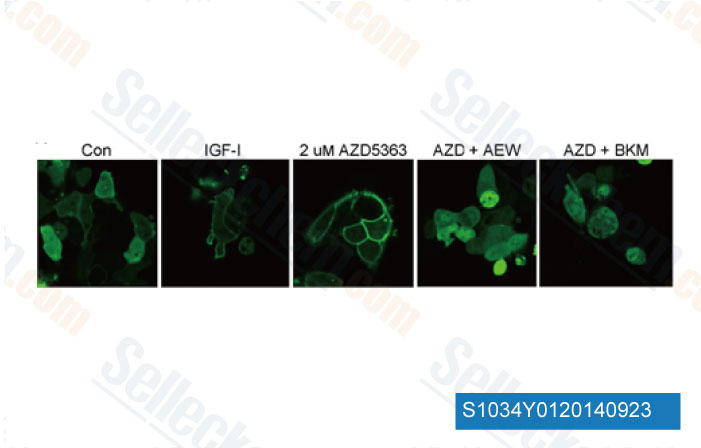
-
Datos de [ Breast Cancer Res , 2013 , 15, R55 ]
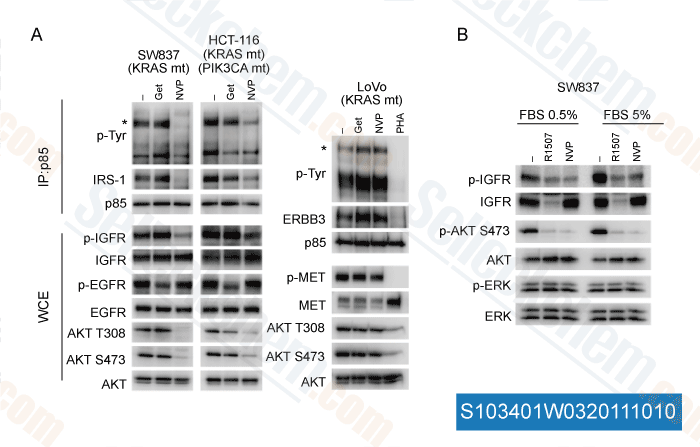
-
Datos de [ J Clin Invest , 2011 , 121, 4311-21 ]
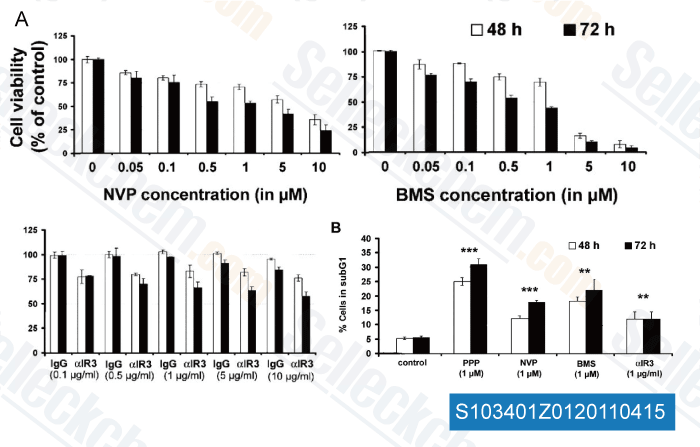
-
Datos de [ Clin Cancer Res , 2011 , 17, 2237-2249 ]
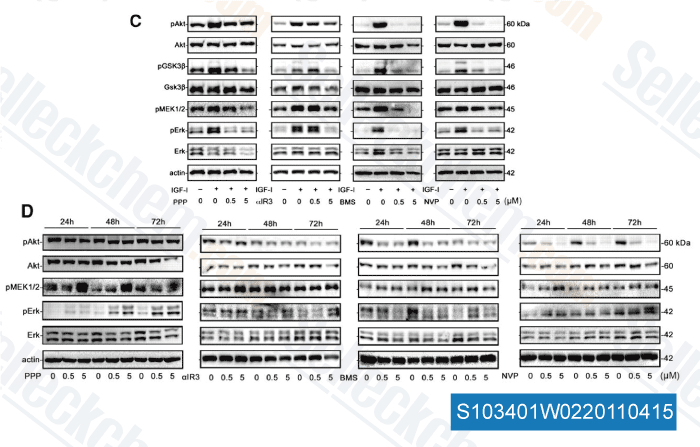
-
Datos de [ Clin Cancer Res , 2011 , 17, 2237-2249 ]
Sellecks NVP-AEW541 Ha sido citado por 67 Publicaciones
| Translocation of IGF-1R in endoplasmic reticulum enhances SERCA2 activity to trigger Ca2+ER perturbation in hepatocellular carcinoma [ Acta Pharm Sin B, 2023, 13(9):3744-3755] | PubMed: 37719369 |
| Anatomic position determines oncogenic specificity in melanoma [ Nature, 2022, 604(7905):354-361] | PubMed: 35355015 |
| Integrative analysis of drug response and clinical outcome in acute myeloid leukemia [ Cancer Cell, 2022, S1535-6108(22)00312-9] | PubMed: 35868306 |
| SFRP4+ stromal cell subpopulation with IGF1 signaling in human endometrial regeneration [ Cell Discov, 2022, 8(1):95] | PubMed: 36163341 |
| Comprehensive drug response profiling and pan-omic analysis identified therapeutic candidates and prognostic biomarkers for Asian cholangiocarcinoma [ iScience, 2022, 25(10):105182] | PubMed: 36248745 |
| Strong Synergic Growth Inhibition and Death Induction of Cancer Cells by Astragalus membranaceus and Vaccaria hispanica Extract [ Cancers (Basel), 2022, 14(23)5833] | PubMed: 36497315 |
| Differential cytotoxic activity of pharmacological inhibitors of IGF1R-related pathways in JAK2V617F driven cells [ Toxicol In Vitro, 2022, 83:105384] | PubMed: 35568132 |
| Targeting Aurora B kinase prevents and overcomes resistance to EGFR inhibitors in lung cancer by enhancing BIM- and PUMA-mediated apoptosis [ Cancer Cell, 2021, S1535-6108(21)00383-4] | PubMed: 34388376 |
| Three subtypes of lung cancer fibroblasts define distinct therapeutic paradigms [ Cancer Cell, 2021, S1535-6108(21)00492-X] | PubMed: 34624218 |
| Aerobic exercise and resistance exercise alleviate skeletal muscle atrophy through IGF-1/IGF-1R-PI3K/Akt pathway in mice with myocardial infarction [ Am J Physiol Cell Physiol, 2021, 10.1152/ajpcell.00344.2021] | PubMed: 34852207 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
