Datos técnicos
| Fórmula | C14H19BCl2N2O4 |
||||||
| Peso molecular | 361.03 | Número CAS | 1072833-77-2 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 72 mg/mL (199.42 mM) | ||||
| Ethanol | 72 mg/mL (199.42 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Ixazomib (MLN2238) inhibe el sitio proteolítico (β5) similar a la quimotripsina del 20S proteasome con IC50 y Ki de 3,4 nM y 0,93 nM en ensayos sin células, respectivamente; también inhibe los sitios proteolíticos similares a la caspasa (β1) y similares a la tripsina (β2), con IC50 de 31 y 3500 nM. Ixazomib (MLN2238) induce la autophagy. Fase 3. | ||||
|---|---|---|---|---|---|
| Objetivos |
|
||||
| In vitro | A concentraciones más altas, este compuesto también inhibe los sitios proteolíticos de tipo caspasa (β1) y de tipo tripsina (β2) con IC50 de 31 nM y 3,5 uM, respectivamente. Inhibe la célula Calu-6 con IC50 de 9,7 nM. MLN2238 es un inhibidor selectivo, potente y reversible del Proteasome en células tumorales. Este compuesto muestra una inhibición del Proteasome reversible dependiente del tiempo. Tanto este compuesto como Bortezomib muestran una inhibición del Proteasome reversible dependiente del tiempo; sin embargo, la vida media de disociación del Proteasome para este se determina que es ~6 veces más rápida que la de Bortezomib (18 y 110 minutos, respectivamente). Se disocia más rápidamente del Proteasome que Bortezomib, lo que es consistente con una recuperación más rápida de la actividad del Proteasome observada en el ensayo Proteasome-Glo. Tiene un mayor efecto farmacodinámico tumoral general que Bortezomib, según lo evaluado por la inhibición del 20S. Este compuesto es la forma biológicamente activa de MLN9708. | ||||
| In vivo | MLN2238 induce una mayor respuesta farmacodinámica que Bortezomib en tumores de xenoinjerto. Este compuesto muestra una mayor inhibición máxima y sostenida del Proteasome tumoral en comparación con Bortezomib en modelos de xenoinjerto. Estos resultados confirman que la mejor exposición tumoral observada con este agente se traduce en una mejor respuesta farmacodinámica tumoral tanto a nivel como aguas abajo del Proteasome. Muestra actividad antitumoral en el modelo de xenoinjerto CWR22. Este químico muestra mayores respuestas farmacodinámicas tumorales en xenoinjertos WSU-DLCL2 en comparación con Bortezomib. De manera similar, el tratamiento con Bortezomib solo condujo a un aumento menor en los niveles de GADD34 en los tumores de xenoinjerto WSU-DLCL2, mientras que este induce fuertemente su expresión. Este compuesto tiene un perfil farmacodinámico y una actividad antitumoral mejorados en comparación con Bortezomib en ambos modelos OCI-Ly10 y PHTX22L. | ||||
| Características | Un inhibidor de Proteasome de primera clase que ha mejorado la farmacocinética (PK), la farmacodinámica (PD) y la actividad antitumoral en estudios preclínicos. |
Protocolo (de referencia)
| Ensayo de quinasa:[1] |
|
|---|---|
| Ensayo celular:[1] |
|
| Estudio en animales:[2] |
|
Referencias
|
Validación de productos por parte del cliente
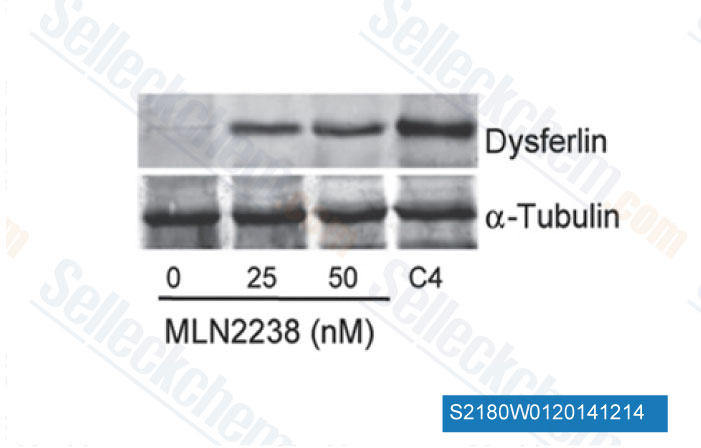
-
Datos de [ Sci Transl Med , 2014 , 6(250), 250ra112 ]
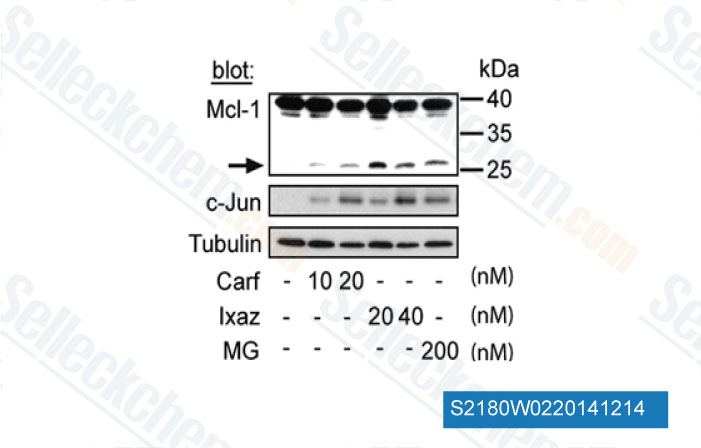
-
Datos de [ Cancer Lett , 2014 , 343(2), 286-94 ]
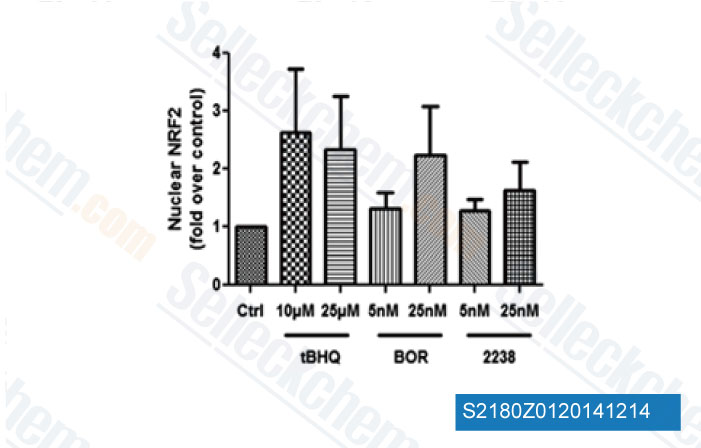
-
Datos de [ Hemoglobin , 2014 , 38(3), 188-95 ]
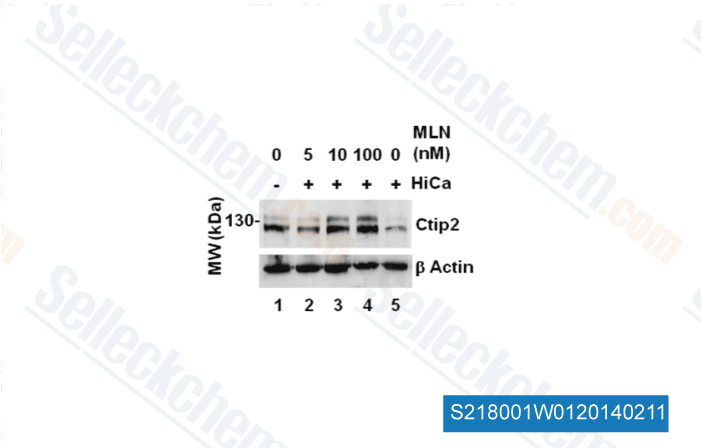
-
Datos de [ J Cell Sci , 2012 , 125(Pt 23), 5733-44 ]
Sellecks MLN2238 (Ixazomib) Ha sido citado por 71 Publicaciones
| Structural basis for allosteric modulation of M. tuberculosis proteasome core particle [ Nat Commun, 2025, 16(1):3138] | PubMed: 40169579 |
| A patient-derived T cell lymphoma biorepository uncovers pathogenetic mechanisms and host-related therapeutic vulnerabilities [ Cell Rep Med, 2025, S2666-3791(25)00102-8] | PubMed: 40147445 |
| Enhancing T cell cytotoxicity in multiple myeloma with bispecific αPD-L1 × αCD3 T cell engager-armed T cells and low-dose bortezomib therapy [ Biomed Pharmacother, 2025, 184:117878] | PubMed: 39891948 |
| High-Throughput Drug Screening of Clear Cell Ovarian Cancer Organoids Reveals Vulnerability to Proteasome Inhibitors and Dinaciclib and Identifies AGR2 as a Therapeutic Target [ Cancer Res Commun, 2025, 5(6):1018-1033] | PubMed: 40459063 |
| Integrated transcriptomics- and structure-based drug repositioning identifies drugs with proteasome inhibitor properties [ Sci Rep, 2024, 14(1):18772] | PubMed: 39138277 |
| A combinatorial therapeutic approach to enhance FLT3-ITD AML treatment [ Cell Rep Med, 2023, 10.1016/j.xcrm.2023.101286] | PubMed: 37951217 |
| Targeting ITGB4/SOX2-driven lung cancer stem cells using proteasome inhibitors [ iScience, 2023, 26(8):107302] | PubMed: 37554452 |
| Dual inhibition of HSF1 and DYRK2 impedes cancer progression [ Biosci Rep, 2023, 43(1)BSR20222102] | PubMed: 36622366 |
| Proteasome inhibition as a therapeutic target for the fungal pathogen Cryptococcus neoformans [ Microbiol Spectr, 2023, 11(5):e0190423] | PubMed: 37750732 |
| Proteasome inhibition as a therapeutic target for the fungal pathogen Cryptococcus neoformans [ Microbiol Spectr, 2023, 10.1128/spectrum.01904-23] | PubMed: 37750732 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
