Datos técnicos
| Fórmula | C20H20N4O |
||||||||||
| Peso molecular | 332.4 | Número CAS | 1000669-72-6 | ||||||||
| Solubilidad (25°C)* | In vitro | DMSO | 67 mg/mL (201.56 mM) | ||||||||
| Ethanol | 67 mg/mL (201.56 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | KW-2449 es un inhibidor multi-dirigido, principalmente para Flt3 con un IC50 de 6.6 nM, modestamente potente para FGFR1, Bcr-Abl y Aurora A; poco efecto sobre PDGFRβ, IGF-1R, EGFR. Fase 1. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
|||||||||||
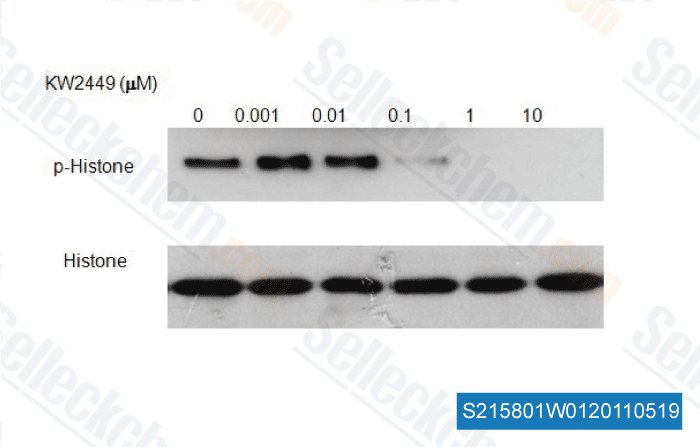
| In vitro | KW-2449, un inhibidor multiquinasa de FLT3, ABL, ABL-T315I y Aurora kinase, está siendo investigado para tratar a pacientes con leucemia. Este compuesto muestra potentes efectos inhibidores del crecimiento en células de leucemia con mutaciones de FLT3 mediante la inhibición de la quinasa FLT3, lo que resulta en la regulación a la baja de FLT3/STAT5 fosforilado, detención en G1 y apoptosis. La administración oral de este químico muestra una inhibición del crecimiento tumoral dosis-dependiente y significativa en modelos de xenoinjerto con mutación de FLT3 con una supresión mínima de la médula ósea. En la leucemia humana de tipo salvaje FLT3, induce la reducción de la histona H3 fosforilada, la detención en G2/M y la apoptosis. En la leucemia resistente a Imatinib, este agente contribuye a liberar la resistencia mediante la regulación a la baja simultánea de las quinasas BCR/ABL y Aurora. La actividad inhibidora de este compuesto no se ve afectada por la presencia de proteínas plasmáticas humanas, como la glicoproteína α1-ácida. Tiene una potente actividad inhibidora del crecimiento contra varios tipos de leucemia por varios mecanismos de acción. Este inhibidor tiene una actividad significativa y justifica un estudio clínico en pacientes con leucemia con mutaciones de FLT3, así como mutaciones resistentes a Imatinib. Los niveles de fosforilación de FLT3 y STAT5 disminuyen por este químico de manera dosis-dependiente. Además, inhibe potentemente ABL-T315I, que se asocia con resistencia a IM, con un IC50 de 4 nM. Por otro lado, este compuesto tiene poco efecto sobre PDGFRβ, IGF-1R, EGFR y varias serina/treonina quinasas incluso a una concentración de 1 μM. Tiene potentes actividades inhibidoras del crecimiento no solo contra células de leucemia que expresan FLT3/ITD, sino también contra células de leucemia activadas por FLT3/KDM y células de leucemia que sobreexpresan FLT3 de tipo salvaje. De acuerdo con el efecto inhibidor del crecimiento, este agente suprime las fosforilaciones de FLT3 (P-FLT3) y su molécula aguas abajo fosfo-STAT5 (P-STAT5) en células MOLM-13 de manera dosis-dependiente. Además, aumenta el porcentaje de células en la fase G1 del ciclo celular y reduce recíprocamente el porcentaje de células en la fase S, lo que resulta en el aumento de la población de células apoptóticas. Este compuesto puede desfosforilar la quinasa WT-FLT3 constitutivamente activa, pero no inhibe la proliferación de células de leucemia si no son principalmente adictas a la quinasa FLT3. Se absorbe rápidamente y se convierte en un metabolito principal M1. Los estudios preclínicos revelan que este químico es convertido por la monoamino oxidasa-B (MAO-B) y la aldehído oxidasa en su principal metabolito M1. Este agente media la citotoxicidad mediante la inhibición de FLT3/ITD. Es un inhibidor directo de FLT3 e induce la inhibición de su objetivo aguas abajo STAT5. Este compuesto interactúa sinérgicamente con los HDACIs para inducir apoptosis en células de LMC Ph+ de manera dependiente del tiempo y la concentración. Mejora sinérgicamente la letalidad de vorinostat/SNDX275 en células de LMC. Estos regímenes inhibidores son activos contra células de leucemia Bcr/Abl+ adicionales resistentes a IM. Reduce moderadamente la fosforilación de la histona H3, un indicador de la actividad de Aurora B, en células K562 tratadas con nocodazol. | |||||||||||
| In vivo | En el modelo de xenoinjerto tumoral MOLM-13, la administración oral de KW-2449 durante 14 días muestra un potente y significativo efecto antitumoral de manera dosis-dependiente. | |||||||||||
| Características | Investigado como FLT3 inhibitor en ensayos clínicos, con otros en desarrollo temprano. |
Protocolo (de referencia)
| Ensayo de quinasa:[2] |
|
|---|---|
| Ensayo celular: [1] |
|
| Estudio en animales:[3] |
|
Referencias
|
Validación de productos por parte del cliente
-
, , Dr. Zhang of Tianjin Medical University
Sellecks KW-2449 Ha sido citado por 12 Publicaciones
| Integrative analysis of drug response and clinical outcome in acute myeloid leukemia [ Cancer Cell, 2022, S1535-6108(22)00312-9] | PubMed: 35868306 |
| A community challenge for a pancancer drug mechanism of action inference from perturbational profile data [ Cell Rep Med, 2022, 3(1):100492] | PubMed: 35106508 |
| Phosphorylation of SHP2 at Tyr62 Enables Acquired Resistance to SHP2 Allosteric Inhibitors in FLT3-ITD-Driven AML [ Cancer Res, 2022, 82(11):2141-2155] | PubMed: 35311954 |
| KW-2449 and VPA exert therapeutic effects on human neurons and cerebral organoids derived from MECP2-null hESCs [ Stem Cell Res Ther, 2022, 13(1):534] | PubMed: 36575558 |
| Evaluation of CML TKI Induced Cardiovascular Toxicity and Development of Potential Rescue Strategies in a Zebrafish Model [ Front Pharmacol, 2021, 12:740529] | PubMed: 34733159 |
| Mechanisms of Oncogenesis in the Primary Liver Cell Cancer [ DTIC, 2021, 53] | PubMed: None |
| The Global Phosphorylation Landscape of SARS-CoV-2 Infection [ Cell, 2020, 182(3):685-712.e19] | PubMed: 32645325 |
| Synergistic Anti Leukemia Effect of a Novel Hsp90 and a Pan Cyclin Dependent Kinase Inhibitors. [ Molecules, 2020, 8;25(9) pii: E2220] | PubMed: 32397330 |
| Small-Molecule and CRISPR Screening Converge to Reveal Receptor Tyrosine Kinase Dependencies in Pediatric Rhabdoid Tumors. [ Cell Rep, 2019, 28(9):2331-2344] | PubMed: 31461650 |
| Drug Target Commons: A Community Effort to Build a Consensus Knowledge Base for Drug-Target Interactions [Tang J Cell Chem Biol, 2018, 25(2):224-229] | PubMed: 29276046 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
