Datos técnicos
| Fórmula | C26H27NO9.HCl |
||||||
| Peso molecular | 533.95 | Número CAS | 57852-57-0 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 100 mg/mL (187.28 mM) | ||||
| Water | 5 mg/mL (9.36 mM) | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Idarubicin HCl (4-demetoxidaunorubicina (NSC256439, 4-DMDR) HCl) es una forma de sal de clorhidrato de Idarubicin, que es un antibiótico de antraciclina y un inhibidor de la DNA topoisomerase II (topo II) para células MCF-7 con una IC50 de 3,3 ng/mL en un ensayo sin células. Idarubicin induce autophagy citotóxica dependiente de mTOR. | ||||
|---|---|---|---|---|---|
| Objetivos |
|
||||
| In vitro | Idarubicin tiene una actividad citotóxica significativa contra esferoides multicelulares, comparable a los efectos antiproliferativos en células monocapa. Idarubicin inhibe el CYP450 2D6. Idarubicin es aproximadamente 57,5 veces y 25 veces más activa que la doxorrubicina y la epirrubicina, respectivamente. Idarubicin es capaz de superar la resistencia a múltiples fármacos mediada por la P-glicoproteína. Idarubicin inhibe la formación de radicales superóxido de PMN. Idarubicin podría acoplarse a los anticuerpos monoclonales (anti-Ly-2.1, anti-L3T4 o anti-Thy-1) con retención de la solubilidad proteica y la actividad de los anticuerpos. Idarubicin inhibe la proliferación de células NALM-6 con una IC50 de 12 nM. |
||||
| In vivo | La reducción de Idarubicin depende de las cetonas reductasas y procede de manera más estereoselectiva que la de la mayoría de las cetonas, dando lugar casi exclusivamente al epímero (13S). La alta estereoselectividad en la reducción de Idarubicin podría resultar de la inducción quiral debido a la presencia de centros asimétricos cerca del grupo carbonilo en Idarubicin. |
||||
| Características | Idarubicin es un sustrato para CYP450 2D6 y 2C9. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
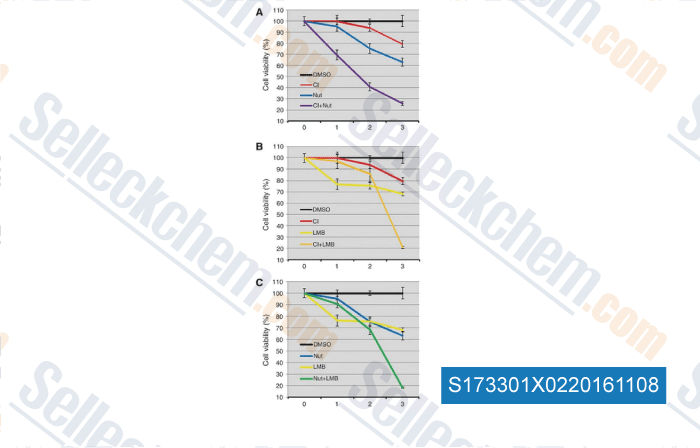
-
, , Clin Cancer Res, 2016, 22(3):746-56.
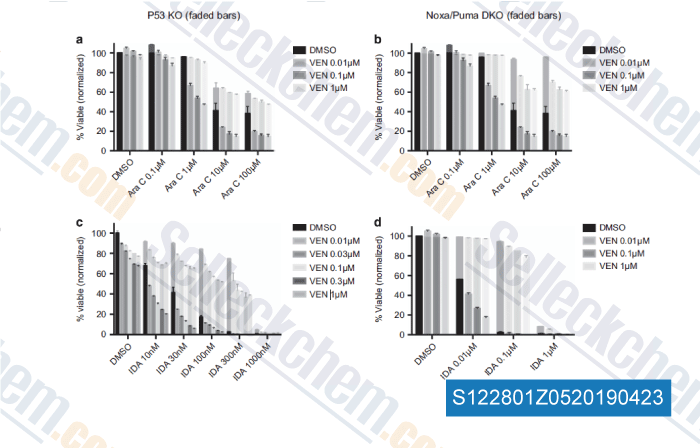
-
Datos de [ , , Leukemia, 2018, 32(2):303-312 ]
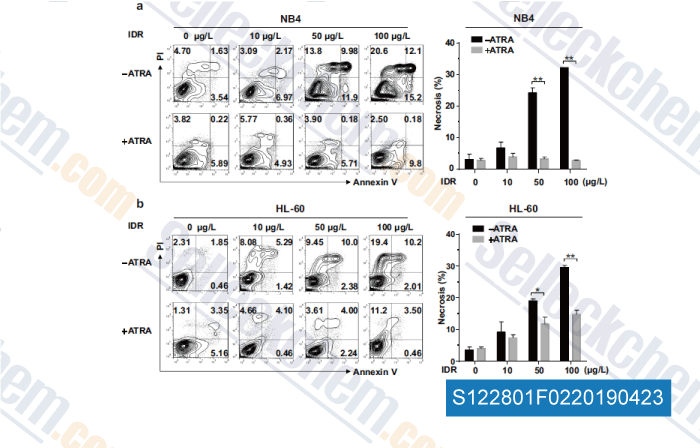
-
Datos de [ , , Mol Cell Biochem, 2018, doi:10.1007/s11010-018-3402-0 ]
Sellecks Idarubicin HCl Ha sido citado por 58 Publicaciones
| An isoform-specific RUNX1C-BTG2 axis governs AML quiescence and chemoresistance [ Blood Cancer Discov, 2025, 10.1158/2643-3230.BCD-24-0327] | PubMed: 40632085 |
| An Isoform-Specific RUNX1C-BTG2 Axis Governs AML Quiescence and Chemoresistance [ Blood Cancer Discov, 2025, 6(5):464-483] | PubMed: 40632085 |
| Relevance of transportome among the mechanisms of chemoresistance in hepatoblastoma [ Biochem Pharmacol, 2025, 237:116914] | PubMed: 40185314 |
| G2 arrest primes hematopoietic stem cells for megakaryopoiesis [ Cell Rep, 2024, 43(7):114388] | PubMed: 38935497 |
| Patient-derived rhabdomyosarcoma cells recapitulate the genetic and transcriptomic landscapes of primary tumors [ iScience, 2024, 27(10):110862] | PubMed: 39319271 |
| Immuno-oncological effects of standard anticancer agents and commonly used concomitant drugs: an in vitro assessment [ BMC Pharmacol Toxicol, 2024, 25(1):25] | PubMed: 38444002 |
| Histone H3 lysine 27 crotonylation mediates gene transcriptional repression in chromatin [ Mol Cell, 2023, 83(13):2206-2221.e11] | PubMed: 37311463 |
| Spermatogenesis associated serine rich 2 like plays a prognostic factor and therapeutic target in acute myeloid leukemia by regulating the JAK2/STAT3/STAT5 axis [ J Transl Med, 2023, 21(1):115] | PubMed: 36774517 |
| Relevance of the organic anion transporting polypeptide 1B3 (OATP1B3) in the personalized pharmacological treatment of hepatocellular carcinoma [ Biochem Pharmacol, 2023, 214:115681] | PubMed: 37429423 |
| p53 controls choice between apoptotic and non-apoptotic death following DNA damage [ bioRxiv, 2023, 2023.01.17.524444] | PubMed: 36712034 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
