Datos técnicos
| Fórmula | C23H30N8O3S |
||||||
| Peso molecular | 498.6 | Número CAS | 1032754-93-0 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 27 mg/mL (54.15 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Apitolisib (GDC-0980, RG7422, GNE 390) es un potente inhibidor de PI3K de clase I para PI3Kα/β/δ/γ con una IC50 de 5 nM/27 nM/7 nM/14 nM en ensayos sin células, respectivamente. También actúa como un inhibidor de mTOR con una Ki de 17 nM en un ensayo sin células, y es altamente selectivo frente a otras quinasas de la familia PIKK. Este compuesto activa la autophagy y la Apoptosis simultáneamente en células de cáncer de páncreas. Fase 2. | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
||||||||||
| In vitro | Apitolisib (GDC-0980) muestra actividades inhibitorias potentes y selectivas contra las quinasas PI3K de clase I y mTOR frente a un amplio panel de quinasas, con Ki de 17 nM para mTOR e IC50 de 5 nM, 27 nM, 7 nM y 14 nM para PI3Kα, β, δ y γ, respectivamente. In vitro, este compuesto inhibe significativamente la proliferación celular en células PC3 y MCF7 con IC50 de 307 nM y 255 nM, respectivamente. Un estudio reciente muestra que reduce la viabilidad de las células cancerosas al inhibir la progresión del ciclo celular e inducir la apoptosis con mayor potencia en líneas de próstata (IC50 < 200 nM 50%, <500 nM 100%), mama (IC50 <200 nM 37%, <500 nM 78%) y CPNM (IC50 <200 nM 29%, <500 nM 88%) y menor potencia en líneas celulares de páncreas (IC50 <200 nM 13%, <500 nM 67%) y melanoma (IC50 <200 nM 0%, <500 nM 33%). | ||||||||||
| In vivo | Apitolisib (GDC-0980) exhibe una actividad antitumoral significativa a una dosis de 1 mg/kg, causando un retraso en el crecimiento tumoral en modelos de xenoinjerto PC-3 y MCF-7 neo/HER2. Además, este compuesto produce estasis o regresiones tumorales a la dosis máxima tolerada de 7,5 mg/kg. En ratones, la administración intravenosa a 1 mg/kg conduce a una baja depuración (Clp: 9,2 mL/min/kg, Vss: 1,7 L/kg). Mientras que la administración oral a 5 mg/kg en 80% PEG400 y a 50 mg/kg como una suspensión cristalina en 0,5% metilcelulosa/0,2% Tween-80 también resulta en parámetros farmacocinéticos favorables. | ||||||||||
| Características | Un potente, selectivo y oralmente disponible inhibidor de PI3Kα, β, δ, γ y mTOR. |
Protocolo (de referencia)
| Ensayo de quinasa:[1] |
|
|---|---|
| Ensayo celular:[1] |
|
| Estudio en animales:[1] |
|
Referencias
|
Validación de productos por parte del cliente
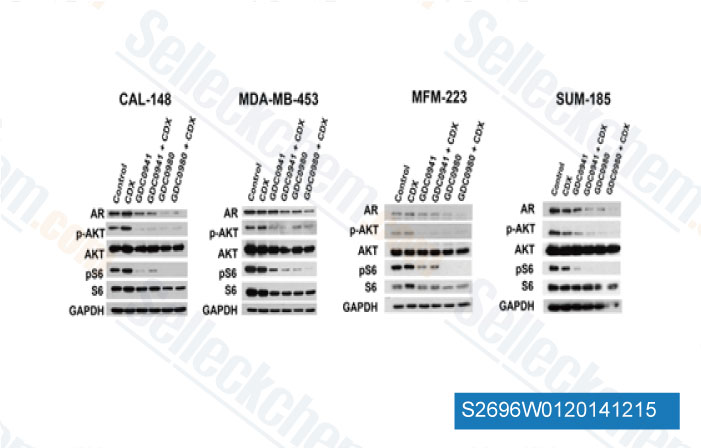
-
Datos de [ Breast Cancer Res , 2014 , 16(4), 406 ]
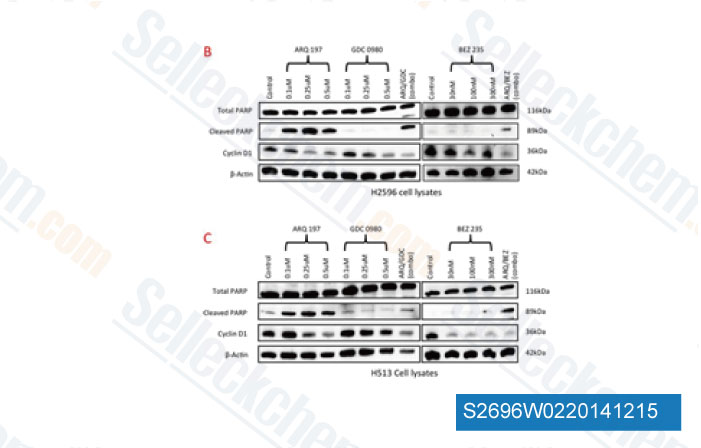
-
Datos de [ PLoS One , 2014 , 9(9), e105919 ]
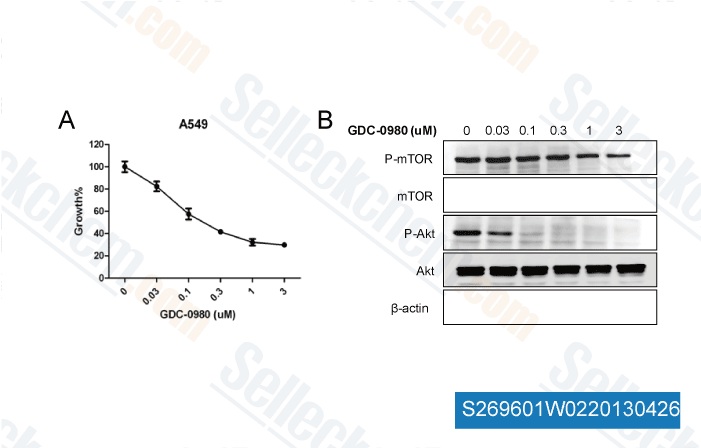
-
, , Dr.Wang Wei from NanFang Hospital
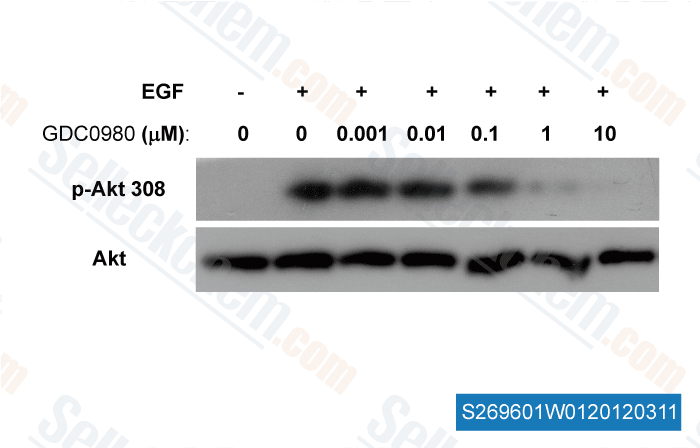
-
, , Dr. Zhang of Tianjin Medical University
Sellecks Apitolisib (GDC-0980) Ha sido citado por 34 Publicaciones
| Depleting the action of EZH2 through PI3K-mTOR inhibition to overcome metastasis and immunotherapy resistance in triple-negative breast cancer [ Mol Cancer Ther, 2025, 10.1158/1535-7163.MCT-24-0693] | PubMed: 40497697 |
| Establishment, characterization, and biobanking of 36 pancreatic cancer organoids: prediction of metastasis in resectable pancreatic cancer [ Cell Oncol (Dordr), 2024, 10.1007/s13402-024-00939-5] | PubMed: 38619751 |
| Dual targeting of the androgen receptor and PI3K/AKT/mTOR pathways in prostate cancer models improves antitumor efficacy and promotes cell apoptosis [ Mol Oncol, 2024, 10.1002/1878-0261.13577] | PubMed: 38225213 |
| Ferroptosis heterogeneity in triple-negative breast cancer reveals an innovative immunotherapy combination strategy [ Cell Metab, 2022, S1550-4131-2200411-9] | PubMed: 36257316 |
| Distinctive molecular features of regenerative stem cells in the damaged male germline [ Nat Commun, 2022, 13(1):2500] | PubMed: 35523793 |
| Overexpression of S100A9 in obesity impairs macrophage differentiation via TLR4-NFkB-signaling worsening inflammation and wound healing [ Theranostics, 2022, 12(4):1659-1682] | PubMed: 35198063 |
| Cancer genes disfavoring T cell immunity identified via integrated systems approach [ Cell Rep, 2022, 40(5):111153] | PubMed: 35926468 |
| Therapeutic Targeting of Stromal-Tumor HGF-MET Signaling in an Organotypic Triple-Negative Breast Tumor Model [ Mol Cancer Res, 2022, 20(7):1166-1177] | PubMed: 35348758 |
| Identification of New Vulnerabilities in Conjunctival Melanoma Using Image-Based High Content Drug Screening [ Cancers (Basel), 2022, 14(6)1575] | PubMed: 35326726 |
| Culture and multiomic analysis of lung cancer patient-derived pleural effusions revealed distinct druggable molecular types [ Sci Rep, 2022, 12(1):6345] | PubMed: 35428753 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
