Datos técnicos
| Fórmula | C21H20ClNO5 |
||||||
| Peso molecular | 401.84 | Número CAS | 146426-40-6 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 80 mg/mL (199.08 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Flavopiridol (Alvocidib) compite con el ATP para inhibir las CDK, incluyendo CDK1, CDK2, CDK4, CDK6 y CDK9 con valores de IC50 en el rango de 20-100 nM. Es más selectivo para CDK1, 2, 4, 6, 9 frente a CDK7. Inicialmente se encuentra que el Flavopiridol inhibe el EGFR y la PKA. El Flavopiridol induce autophagy y estrés del RE. El Flavopiridol bloquea la replicación del HIV-1. Fase 1/2. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
|||||||||||
| In vitro | Flavopiridol (Alvocidib) muestra menor actividad contra quinasas no relacionadas como MAP, PAK, PKC y EGFR con un IC50 de >14 μM. Inhibe significativamente el crecimiento de colonias de células HCT116, A2780, PC3 y Mia PaCa-2 con IC50 de 13 nM, 15 nM, 10 nM y 36 nM, respectivamente. Este compuesto también inhibe potentemente la actividad de la glucógeno sintasa quinasa-3 (GSK-3) con un IC50 de 280 nM. En comparación con otras CDKs, inhibe la actividad de CDK7 con menor potencia, con un IC50 de 875 nM. A 0.5 μM, inhibe tanto pSer807/811 Rb como pThr199 NPM, mientras que se observan cambios leves en pThr821 Rb. También disminuye el nivel general de ARN polimerasa II, así como la fosforilación de la ARN polimerasa II en los repetidos CTD en Ser2 Ser5. Como un inhibidor de CDK de amplio espectro, puede inhibir la progresión del Cell Cycle tanto en G1 como en G2. A 0.3 μM, induce la detención en G1 en células MCF-7 o MDA-MB-468 mediante la inhibición de la actividad quinasa de CDK4 o CDK2. Exhibe una potente citotoxicidad contra una amplia variedad de líneas celulares tumorales con valores de IC50 que van desde 16 nM para LNCAP hasta 130 nM para K562. | |||||||||||
| In vivo | La administración de S1230 a 7.5 mg/kg durante 7 días muestra una ligera actividad antitumoral contra la leucemia murina P388, resultando en un valor %T/C de 110, y es activa contra el carcinoma ovárico humano A2780 implantado subcutáneamente en ratones nude, produciendo una eliminación de 1.5 log de células (LCK). El tratamiento con S1230 a 1-2.5 mg/kg durante 10 días suprime significativamente la artritis inducida por colágeno en ratones de manera dosis-dependiente, al inhibir la hiperplasia sinovial y la destrucción articular, mientras que las concentraciones séricas de anticuerpos anti-colágeno tipo II (CII) y las respuestas proliferativas al CII se mantienen. En los xenoinjertos de Hct116 con p21 intacta en ratones nude, la administración de CPT-11 (100 mg/kg) seguida de S1230 (3 mg/kg) 7 y 16 horas después inhibe significativamente la regresión tumoral en un 86 % y 82 %, respectivamente, mostrando una inhibición > 2 veces en comparación con CPT-11 solo en un 40 %. La combinación produce una tasa de respuesta completa (CR) de aproximadamente el 30 %, en contraste con CPT-11 solo, donde no se encuentra CR. | |||||||||||
| Características | Primer inhibidor de CDK utilizado en ensayos clínicos en humanos. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
-
Datos de [ PNAS , 2011 , 108, 8417 ]
![(A) After mitotic arrest and treatment with the proteasome inhibitor MG132, HeLa cells were treated with the indicated kinase inhibitors The cells were harvested, and the lysates were separated by SDS-PAGE and immunoblotted for phosphorylated RV[S/T]F (p-RV[S/T]F, top). The blot was quantified using ImageJ software and normalized to the mitotic sample (bottom). MLN8054, Aurora A and Aurora B inhibitor; ZM447439 and hesperadin, Aurora B inhibitors; BI2536, PLK1 inhibitor; flavopiridol, CDK1 inhibitor. n = 3. **P < 0.01, paired Student’s t test.](https://file.selleckchem.com/downloads/review/700px/flavopiridol-S123001W0420180614.gif)
-
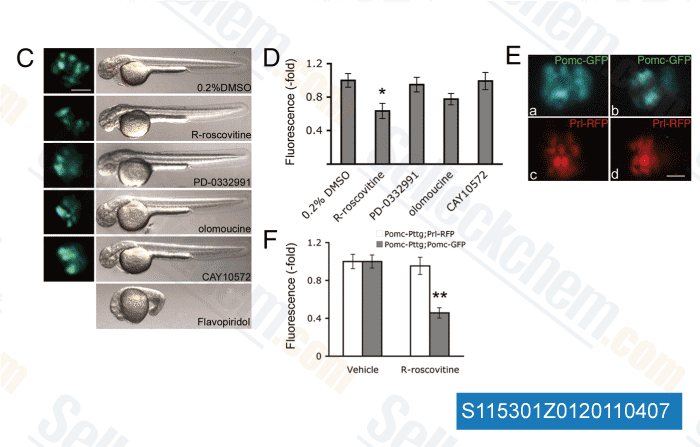
Datos de [ , , Science, 2018, 11(530), doi: 10.1126/scisignal.aai8669 ]
-
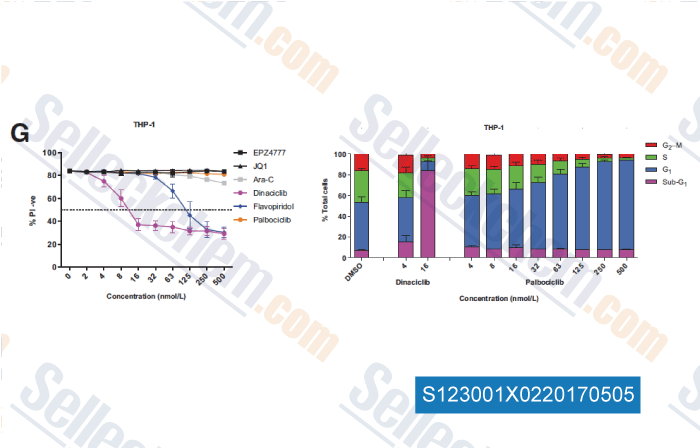
Datos de [ , , Cancer Res, 2016, 76(5):1158-69 ]
-
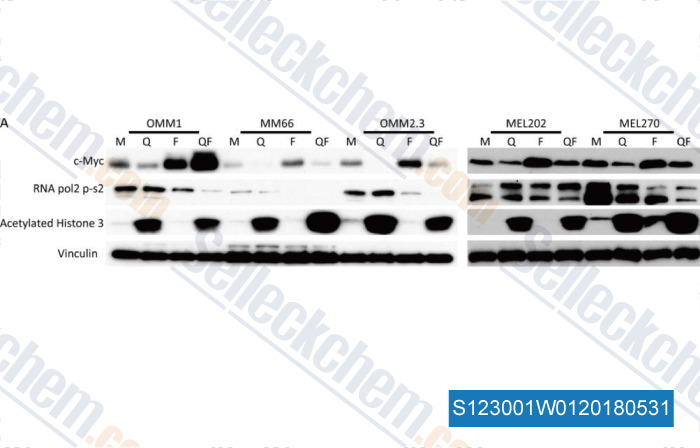
Datos de [ , , Oncotarget, 2018, 9(5): 6174-6187 ]
Sellecks Flavopiridol (Alvocidib, HMR-1275) Ha sido citado por 149 Publicaciones
| SLFN11-mediated ribosome biogenesis impairment induces TP53-independent apoptosis [ Mol Cell, 2025, S1097-2765(25)00042-5] | PubMed: 39909041 |
| Combined therapy with DR5-targeting antibody-drug conjugate and CDK inhibitors as a strategy for advanced colorectal cancer [ Cell Rep Med, 2025, S2666-3791(25)00231-9] | PubMed: 40449480 |
| Maternal CENP-C restores centromere symmetry in mammalian zygotes to ensure proper chromosome segregation [ Dev Cell, 2025, S1534-5807(25)00537-4] | PubMed: 40997799 |
| Identification of modulators of the ALT pathway through a native FISH-based optical screen [ Cell Rep, 2025, 44(1):115114] | PubMed: 39729394 |
| Identifying Age-Modulating Compounds Using a Novel Computational Framework for Evaluating Transcriptional Age [ Aging Cell, 2025, e70075] | PubMed: 40307992 |
| Protection of infant mice against pertussis, tuberculosis and influenza by co-administration of nasal pertussis vaccine candidate BPZE1 and BCG [ iScience, 2025, 28(7):112839] | PubMed: 40612502 |
| Replication-competent adenovirus reporters utilizing endogenous viral expression architecture [ J Virol, 2025, 99(10):e0114625] | PubMed: 40928252 |
| BET degraders reveal BRD4 disruption of 7SK and P-TEFb is critical for effective reactivation of latent HIV in CD4+ T-cells [ J Virol, 2025, 99(4):e0177724] | PubMed: 40067013 |
| Repurposing flavopiridol as an inhaled therapeutic for pulmonary fibrosis [ Eur J Pharmacol, 2025, 1005:178058] | PubMed: 40816528 |
| Bacterial ubiquitin ligase engineered for small molecule and protein target identification [ bioRxiv, 2025, 2025.03.20.644192] | PubMed: 40166235 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
