Datos técnicos
| Fórmula | C21H21FN6O |
||||||
| Peso molecular | 392.43 | Número CAS | 405169-16-6 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 34 mg/mL (86.63 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Dovitinib (TKI-258, CHIR258) es un inhibidor de RTK multidirigido, que se dirige principalmente a los RTK de clase III (FLT3/c-Kit) con valores de IC50 de 1 nM/2 nM. También es potente contra los RTK de clase IV (FGFR1/3) y clase V (VEGFR1-4), exhibiendo valores de IC50 de 8-13 nM, mientras que muestra una menor potencia hacia InsR, EGFR, c-Met, EphA2, Tie2, IGF-1R y HER2 en ensayos libres de células. Fase 4. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
|||||||||||
| In vitro | Dovitinib (TKI-258) inhibe potentemente el crecimiento estimulado por FGF de células B9 que expresan WT y F384L-FGFR3 con una IC50 de 25 nM. Además, inhibe la proliferación de células B9 que expresan cada una de las diversas mutantes activadas de FGFR3. Curiosamente, se observan diferencias mínimas en la sensibilidad de las diferentes mutaciones de FGFR3 a este compuesto, con la IC50 que oscila entre 70 y 90 nM para cada una de las diversas mutaciones. Las células B9 dependientes de IL-6 que contienen solo el vector (células B9-MINV) son resistentes a su actividad inhibidora en concentraciones de hasta 1 µM. Inhibe la proliferación celular de células KMS11 (FGFR3-Y373C), OPM2 (FGFR3-K650E) y KMS18 (FGFR3-G384D) con una IC50 de 90 nM (KMS11 y OPM2) y 550 nM, respectivamente. El compuesto inhibe la fosforilación de ERK1/2 mediada por FGF e induce citotoxicidad en células primarias de MM que expresan FGFR3. Las BMSCs confieren un modesto grado de resistencia con una inhibición del crecimiento del 44,6 % para las células tratadas con 500 nM de Dovitinib y cultivadas en estroma en comparación con una inhibición del crecimiento del 71,6 % para las células cultivadas sin BMSCs. Inhibe la proliferación de M-NFS-60, una línea celular mieloblástica de ratón impulsada por el crecimiento de M-CSF con una concentración efectiva mediana (EC50) de 220 nM. El tratamiento de células SK-HEP1 con este compuesto resulta en una reducción dosis-dependiente del número de células y un arresto en fase G2/M con reducción en las fases G0/G1 y S, inhibición del crecimiento independiente del anclaje y bloqueo de la motilidad celular inducida por bFGF. La IC50 para este compuesto en células SK-HEP1 es aproximadamente de 1,7 µM. También reduce significativamente los niveles de fosforilación basal de FGFR-1, el sustrato 2α de FGFR (FRS2-α) y ERK1/2, pero no de Akt, tanto en células SK-HEP1 como en 21-0208. En células HCC 21-0208, inhibe significativamente la fosforilación inducida por bFGF de FGFR-1, FRS2-α, ERK1/2, pero no de Akt. |
|||||||||||
| In vivo | Dovitinib (TKI-258) induce respuestas tanto citostáticas como citotóxicas in vivo, lo que resulta en la regresión de tumores que expresan FGFR3. Muestra una inhibición dosis y exposición-dependiente de los receptores tirosina quinasas (RTKs) diana expresados en xenoinjertos tumorales. Este compuesto inhibe potentemente el crecimiento tumoral de seis líneas de HCC. La inhibición de la Angiogenesis se correlacionó con la inactivación de las vías de señalización FGFR/PDGFRβ/VEGFR2. En un modelo ortotópico, inhibe potentemente el crecimiento tumoral primario y la metástasis pulmonar y prolonga significativamente la supervivencia de los ratones. La administración de Dovitinib resulta en una inhibición significativa del crecimiento tumoral y regresiones tumorales, incluyendo tumores grandes y establecidos (500-1.000 mm3). |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
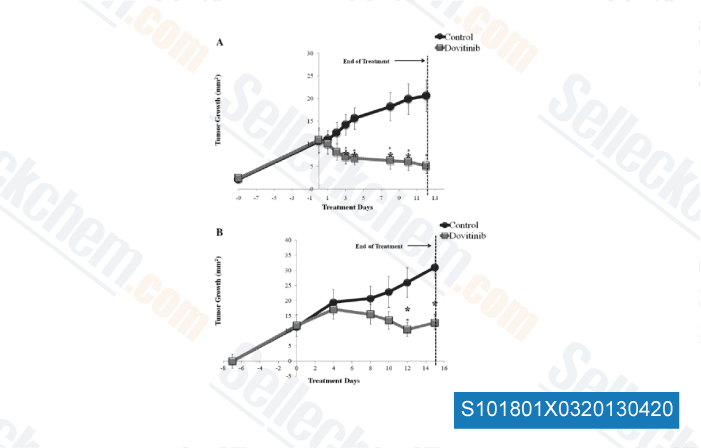
-
Datos de [ Oral Oncol , 2012 , 48, 1242-9 ]
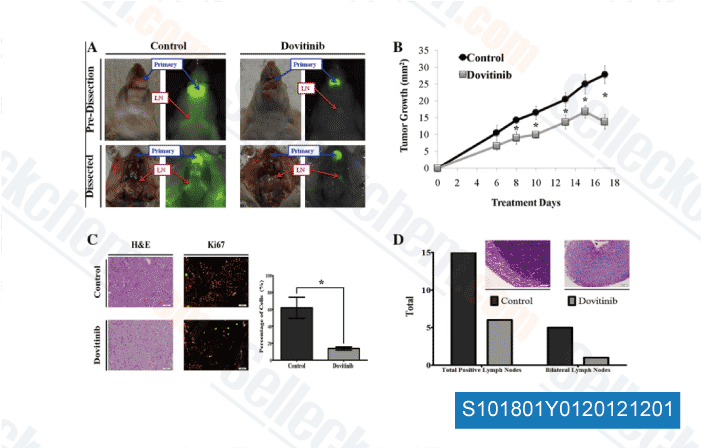
-
Datos de [ Oral Oncol , 2012 , 48, 1242-9 ]
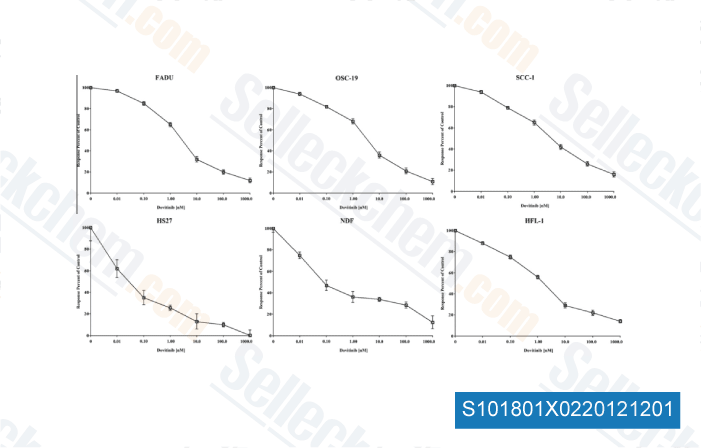
-
Datos de [ Oral Oncol , 2012 , 48, 1242-9 ]
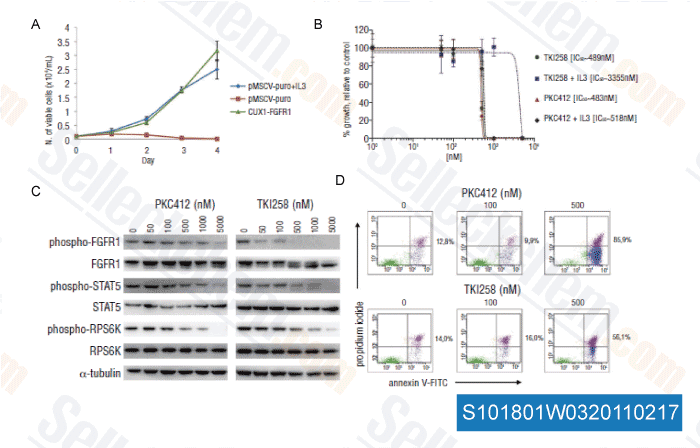
-
Datos de [ Haematologica , 2011 , 96, 922-926 ]
Sellecks Dovitinib (TKI-258) Ha sido citado por 54 Publicaciones
| Characterization of dovitinib-human serum albumin association potential through optical spectroscopic and in silico approaches [ Spectrochim Acta A Mol Biomol Spectrosc, 2025, 343:126602] | PubMed: 40582029 |
| Sensitizing cholangiocarcinoma to chemotherapy by inhibition of the drug-export pump MRP3 [ Biomed Pharmacother, 2024, 180:117533] | PubMed: 39405909 |
| Efficacy of futibatinib, an irreversible fibroblast growth factor receptor inhibitor, in FGFR-altered breast cancer [ Sci Rep, 2023, 13(1):20223] | PubMed: 37980453 |
| CREB3L2-ATF4 heterodimerization defines a transcriptional hub of Alzheimer's disease gene expression linked to neuropathology [ Sci Adv, 2023, 9(9):eadd2671] | PubMed: 36867706 |
| Efeito do tratamento TKI-258 sobre a expressão gênica de seus receptores-alvo e ativação de suas efetoras GTPases Rho em carcinoma epidermoide oral in vitro. [ UFTM, 2023, ] | PubMed: none |
| A community challenge for a pancancer drug mechanism of action inference from perturbational profile data [ Cell Rep Med, 2022, 3(1):100492] | PubMed: 35106508 |
| EGFR-phosphorylated GDH1 harmonizes with RSK2 to drive CREB activation and tumor metastasis in EGFR-activated lung cancer [ Cell Rep, 2022, 41(11):111827] | PubMed: 36516759 |
| Comprehensive drug response profiling and pan-omic analysis identified therapeutic candidates and prognostic biomarkers for Asian cholangiocarcinoma [ iScience, 2022, 25(10):105182] | PubMed: 36248745 |
| Lysine acetylation restricts mutant IDH2 activity to optimize transformation in AML cells [ Mol Cell, 2021, S1097-2765(21)00507-4] | PubMed: 34289383 |
| Targeting fibroblast growth factor receptors to combat aggressive ependymoma [ Acta Neuropathol, 2021, 10.1007/s00401-021-02327-x] | PubMed: 34046693 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
