Datos técnicos
| Fórmula | C25H26ClN5O3 |
||||||
| Peso molecular | 479.96 | Número CAS | 468740-43-4 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 96 mg/mL (200.01 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | BMS-536924 (CS-0117) es un inhibidor de IGF-1R/IR competitivo de ATP con una CI50 de 100 nM/73 nM, actividad modesta para Mek, Fak y Lck con muy poca actividad para Akt1, MAPK1/2. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
|||||||||||
| In vitro | BMS-536924 también inhibe FAK y Lck con una CI50 de 150 nM y 341 nM, respectivamente. Este compuesto inhibe la proliferación celular e interrumpe la fosforilación de Akt y MAPK. Inhibe la señalización de IGF-1R estimulada por IGF-I en células MCF10A y bloquea la actividad constitutiva de IGF-1R en CD8-IGF-1R-MCF10A. La preincubación de células MCF10A con 1 μM de este químico bloquea completamente la capacidad de IGF-I para estimular la fosforilación de IGF-1R. La estimulación con IGF-I da como resultado un aumento de la fosforilación de ERK1/2, GSK3β y Akt. Este compuesto inhibe esta fosforilación inducida por ligando. El tratamiento de las células CD8-IGF-1R-MCF10A con este inhibidor da como resultado una inhibición dosis-dependiente de la fosforilación con inhibición parcial a 0,01 μM y 0,1 μM, pero una inhibición completa del receptor a una concentración de 1 μM. La inhibición máxima de IGF-1R fosforilado se observa tan pronto como 10 minutos después de la incubación. Mantiene su capacidad para inhibir la fosforilación de IGF-1R hasta por 48 horas. La adición de este agente inhibe la fosforilación de Akt de forma dependiente del tiempo a partir de 1 hora. A las 48 horas, la activación de Akt está completamente bloqueada. El tratamiento con este compuesto muestra actividad antiproliferativa en un panel de líneas celulares cancerosas que incluyen las células TC32, HT1080/S, SK-LMS-1, H513 y CTR. pIGF-1R/pIR se activa tras la estimulación con IGF-I/insulina y la activación es inhibida por este químico con potencias similares en las líneas celulares Rh41 y Rh36. La expresión de la muerte celular programada 4 (PDCD4), la escisión de la poli(ADP-ribosa) polimerasa (PARP) y la caspasa-3 se regulan al alza en las células Rh41 tratadas con este inhibidor. | |||||||||||
| In vivo | La administración oral de BMS-536924 a 100-300 mpk inhibe fuertemente el modelo tumoral IGR-1R Sal. También se observa eficacia en el modelo de carcinoma de colon humano Colo205 no modificado genéticamente. La administración oral de este compuesto con una pauta de una vez al día (100-300 mpk) o dos veces al día (50, 100 mpk) demuestra actividad antitumoral en este modelo tumoral. La prueba de tolerancia oral a la glucosa (OGTT) muestra que 100 mpk (b.i.d.) provoca una elevación significativa de los niveles de glucosa después del desafío con glucosa. Los parámetros farmacocinéticos de este químico, administrado por vía oral en poli(etilenglicol) 400 y agua (80:20 v/v), se determinan en ratones, ratas, perros y monos. Se evidencia una buena biodisponibilidad en todas las especies. Se observa una farmacocinética no lineal significativa en roedores con dosis p.o. crecientes. Este compuesto reduce el volumen de los xenoinjertos tumorales de células CD8-IGF-1R-MCF10A después de dos semanas de tratamiento (100 mg/kg) al 76%. La administración oral de 70 mg/kg de este químico inhibe significativamente el crecimiento tumoral (células TGBC-1TKB) inoculadas en ratones nude. Regula al alza la apoptosis en los tumores de xenoinjertos. El tratamiento no tiene efectos adversos sobre el peso corporal de los ratones ni los niveles de glucosa en el momento de la muerte, lo que sugiere una toxicidad tolerable. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
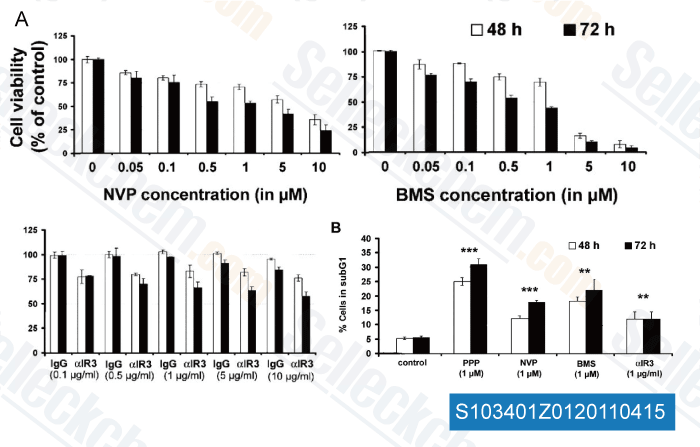
-
Datos de [ Clin Cancer Res , 2011 , 17, 2237-2249 ]
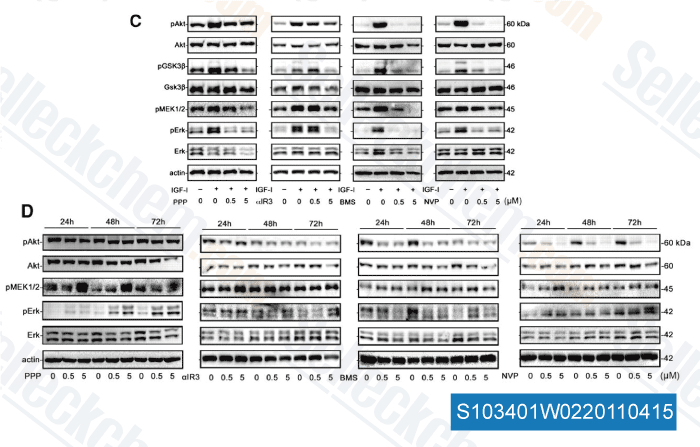
-
Datos de [ Clin Cancer Res , 2011 , 17, 2237-2249 ]
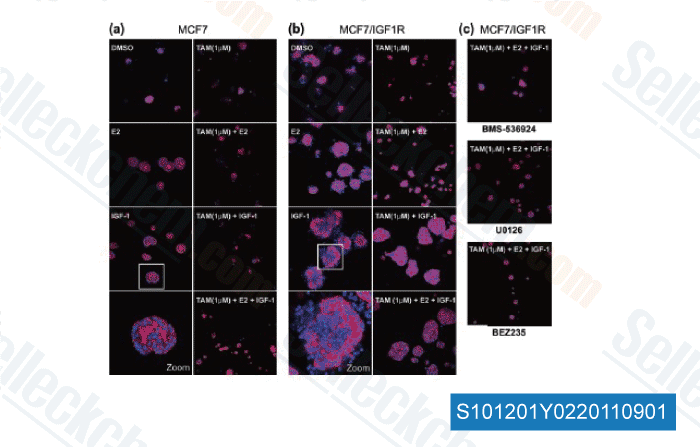
-
Datos de [ Breast Cancer Res , 2011 , 13, R52 ]
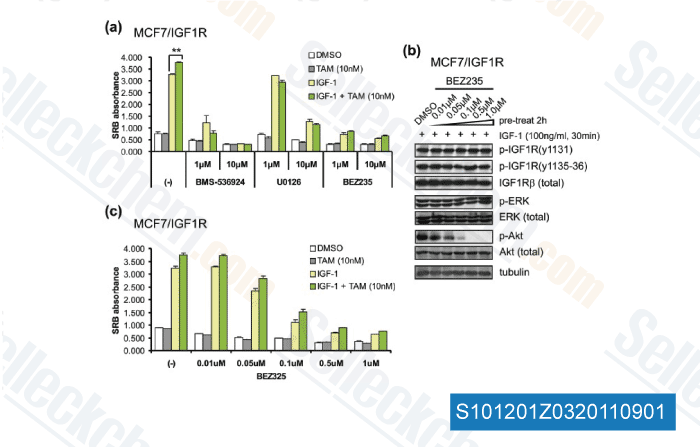
-
Datos de [ Breast Cancer Res , 2011 , 13, R52 ]
Sellecks BMS-536924 Ha sido citado por 27 Publicaciones
| Haploinsufficiency of miR-143 and miR-145 reveal targetable dependencies in resistant del(5q) myelodysplastic neoplasm [ Leukemia, 2025, 39(4):917-928] | PubMed: 40000845 |
| Inhibition of Selenoprotein I promotes ferroptosis and reverses resistance to platinum chemotherapy by impairing Akt phosphorylation in ovarian cancer [ MedComm (2020), 2024, 5(12):e70033] | PubMed: 39669976 |
| High-Content and High-Throughput Clonogenic Survival Assay Using Fluorescence Barcoding [ Cancers -Basel), 2023, 15(19)4772] | PubMed: 37835466 |
| SFRP4+ stromal cell subpopulation with IGF1 signaling in human endometrial regeneration [ Cell Discov, 2022, 8(1):95] | PubMed: 36163341 |
| Multi-omics characterization of autophagy-related molecular features for therapeutic targeting of autophagy [ Nat Commun, 2022, 13(1):6345] | PubMed: 36289218 |
| FER-mediated phosphorylation and PIK3R2 recruitment on IRS4 promotes AKT activation and tumorigenesis in ovarian cancer cells [ Elife, 2022, 11e76183] | PubMed: 35550247 |
| Exosomes from cisplatin-induced dormant cancer cells facilitate the formation of premetastatic niche in bone marrow through activating glycolysis of BMSCs [ Front Oncol, 2022, 12:922465] | PubMed: 36568212 |
| Intermittent parathyroid hormone improves orthodontic retention via insulin-like growth factor-1 [ Oral Dis, 2021, 27(2):290-300] | PubMed: 32608117 |
| Manganese Acts upon Insulin/IGF Receptors to Phosphorylate AKT and Increase Glucose Uptake in Huntington's Disease Cells [ Mol Neurobiol, 2020, 57(3):1570-1593] | PubMed: 31797328 |
| Loss of N-Glycanase 1 Alters Transcriptional and Translational Regulation in K562 Cell Lines [ G3 (Bethesda), 2020, 4;10(5):1585-1597] | PubMed: 32265286 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
