réservé à la recherche
Pantoprazole Proton Pump inhibiteur
N° Cat.S2105
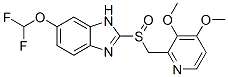
Structure chimique
Poids moléculaire: 383.37
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- SDS
- Fiche technique
| Cibles apparentées | CFTR CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase |
|---|---|
| Autre Proton Pump Inhibiteurs | Bafilomycin A1 (Baf-A1) Ilaprazole Tenatoprazole Revaprazan Hydrochloride Ilaprazole sodium PF-3716556 Ufiprazole |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 383.37 | Formule | C16H15F2N3O4S |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 102625-70-7 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | SKFSKF96022, BY-1023 | Smiles | COC1=C(C(=NC=C1)CS(=O)C2=NC3=C(N2)C=C(C=C3)OC(F)F)OC | ||
Solubilité
|
In vitro |
DMSO
: 76 mg/mL
(198.24 mM)
Ethanol : 76 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
(H+/K+)-ATPase
Proton pump
|
|---|---|
| In vitro |
Le PPZ (Pantoprazole) inhibe la prolifération des cellules tumorales, induit l'apoptose et régule à la baisse l'expression de PKM2, ce qui contribue à la compréhension actuelle de l'association fonctionnelle entre le PPZ et PKM2 (The human M2 isoform of pyruvate kinase). Des études ex vivo ont montré que le pantoprazole inhibait les activités de TOPK dans les cellules JB6 Cl41 et les cellules de cancer colorectal HCT 116. De plus, le knockdown de TOPK dans les cellules HCT 116 a diminué leurs sensibilités au pantoprazole.
|
| In vivo |
L'injection i.p. de pantoprazole chez des souris porteuses de tumeurs colorectales HCT 116 supprime efficacement la croissance du cancer. La molécule de signalisation en aval de TOPK, la phospho-histone H3 dans les tissus tumoraux, est également diminuée après un traitement au pantoprazole. À des débits de perfusion plus élevés, le pantoprazole est capable d'induire des réponses hémodynamiques négatives, en particulier dans le contexte d'une insuffisance cardiaque. Ces effets peuvent entraîner une altération significative de la fonction cardiaque. De plus, le pantoprazole retarde la guérison des fractures en affectant à la fois la formation osseuse et le remodelage osseux.
|
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT04248335 | Recruiting | Pediatric Obesity|NAFLD|GERD |
Children''s Mercy Hospital Kansas City |
July 3 2018 | Phase 4 |
| NCT02401035 | Terminated | Gastroesophageal Reflux Disease |
Pfizer |
May 9 2017 | Phase 4 |
| NCT02274961 | Unknown status | Non Erosive Reflux Disease |
Ahn-Gook Pharmaceuticals Co.Ltd |
October 2014 | Phase 3 |
| NCT02186652 | Completed | Gastroesophageal Reflux Disease |
Phillip Brian Smith|The Emmes Company LLC|Duke University |
June 4 2014 | Phase 1 |
| NCT01710462 | Withdrawn | Gastroesophageal Reflux Disease |
Eurofarma Laboratorios S.A. |
August 2013 | Phase 3 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
