réservé à la recherche
Lomibuvir (VX-222) HCV Protease inhibiteur
N° Cat.S1480
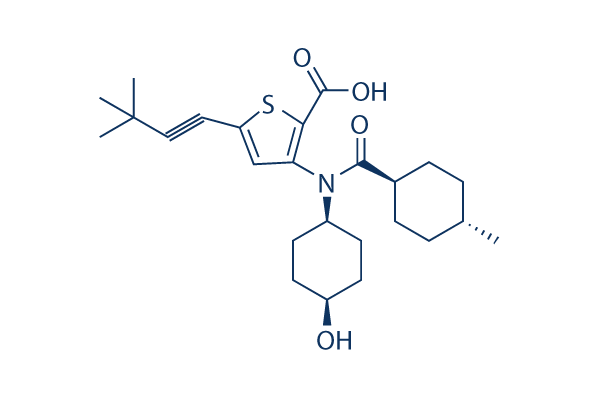
Structure chimique
Poids moléculaire: 445.61
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- HPLC
- SDS
- Fiche technique
| Cibles apparentées | HDAC Caspase Proteasome Secretase MMP Cysteine Protease DPP Tyrosinase HIV Protease Serine Protease |
|---|---|
| Autre HCV Protease Inhibiteurs | Danoprevir Asunaprevir Tizoxanide PSI-6206 (GS-331007) Mecarbinate Tegobuvir Herba taxilli Extract 2'-C-Methylcytidine |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 445.61 | Formule | C25H35NO4S |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 1026785-59-0 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | VCH-222 | Smiles | CC1CCC(CC1)C(=O)N(C2CCC(CC2)O)C3=C(SC(=C3)C#CC(C)(C)C)C(=O)O | ||
Solubilité
|
In vitro |
DMSO
: 89 mg/mL
(199.72 mM)
Ethanol : 89 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Fonctionnalités |
A novel, potent and selective inhibitor of non-nucleoside polymerase, specifically the HCV RNA-dependent RNA polymerase.
|
|---|---|
| Targets/IC50/Ki |
HCV NS5B 1a
0.94 μM
HCV NS5B 1b
1.2 μM
|
| In vitro |
Lomibuvir (VX-222) se lie à la poche allostérique du pouce II de la polymérase ARN-dépendante de l'ARN du HCV. Il présente une inhibition non-compétitive et sélective de la NS5B du HCV de génotype 1a et 1b, avec des IC50 de 0.94 et 1.2 μM, respectivement. Ce composé inhibe sélectivement la réplication du réplicon sous-génomique du HCV de génotype 1a et 1b avec une EC50 de 22.3 et 11.2 nM, respectivement.
De même, une étude récente montre qu'il inhibe le réplicon sous-génomique 1b/Con1 du HCV, avec une EC50 de 5 nM. Le VX-222 inhibe préférentiellement la synthèse d'ARN dépendante de l'amorce, montrant seulement un effet modeste ou nul sur la synthèse d'ARN initiée de novo.
|
| Kinase Assay |
Essai d'activité anti-NS5B
|
|
L'effet inhibiteur du Lomibuvir (VX-222) sur l'activité de la NS5B du HCV est mesuré en évaluant la quantité d'UTP radiomarqué incorporé par la version tronquée ∆21 C-terminale de l'enzyme dans un ARN nouvellement synthétisé en utilisant un modèle/amorce d'ARN homopolymérique, à savoir poly rA / oligo dT. La détection quantitative de la radioactivité incorporée est réalisée à l'aide d'un compteur à scintillation liquide. La cinétique in vitro de l'inhibition de la NS5B du HCV de la souche 1b BK par ce composé est déterminée en utilisant la version tronquée ∆21 C-terminale de la NS5B. Il (1 à 1.5 μM) est testé en présence de 10 à 75 μM d'UTP non radioactif mélangé avec 0.89 à 6.70 μCi d'UTP marqué au [α-33P]. Les réactions de polymérase ARN-dépendante de l'ARN sont laissées se dérouler pendant 18 min à 22 °C.
|
|
| In vivo |
Lomibuvir (VX-222) présente un excellent profil pharmacocinétique chez les rats et les chiens, incluant une faible clairance corporelle totale et une excellente biodisponibilité orale (supérieure à 30%) avec de bonnes propriétés ADME. Il est biotransformé par plusieurs enzymes (CYP1A1, 2A6, 2B6, 2C8, CYP 3A4, UGT1A3) et est prédit être activement transporté dans le foie et excrété principalement intact dans la bile ou sous forme d'adduits glucuronides.
|
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT00958152 | Completed | Hepatitis C |
Vertex Pharmaceuticals Incorporated |
August 2009 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
